Cours spectroscopie infrarouge
1 Spectroscopie Infrarouge
1.7 Les molécules en vibrations suite
Leurs intensités dépendent des populations des niveaux de rotation concernés (fonction de J).
II.2- VIBRATION DES MOLECULES POLYATOMIQUES
II.1 - Modes normaux de vibration
Molécule polyatomique est équivalente à des masses ponctuelles réunies ensemble par des ressorts.
II.1.1 Molécule de N atomes reçoit de l’énergie :
il en résulte un mouvement de vibration compliqué, décomposé en mouvements plus simples appelés
a) MODES NORMAUX DE VIBRATION
Nombre de modes normaux de vibration d'une molécule
Exemple: Les modes normaux de vibration de Al2Cl6
II.2 - Vibrations actives ou inactives - vibrations dégénérées
II.2.1 - Activité
Les mouvements de vibration ne sont pas tous actifs en infrarouge.
Vibration active en spectroscopie IR dépend de la variation du moment dipolaire
Exemple : La molécule de CO2
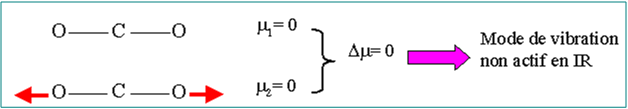
II.2.2 - La dégénérescence
Modes de doublement ou triplement dégénérés : Ce sont des modes ayant la même fréquence de vibration.
II.3 - Vibrations fondamentales
On appelle vibration fondamentale une vibration dont la fréquence correspond à celle d’un mode normal de vibration.
Théoriquement : (3n-6) ou (3n-5) vibrations fondamentales
Actives seulement si variation du moment dipolaire
II.3.1 Allure d’un spectre infrarouge
Spectre IR = Suite de bandes d’absorption, plus ou moins larges
Abscisse : en cm-1
Ordonnée : Transmittance (%T) ou Absorbance A = log(1/T)
Sur le spectre IR, on observe :
Certaines vibrations fondamentales sont absentes sur le spectre IR en raison de leur inactivité.
Mais d’autres bandes d'absorption apparaîssent.
Bandes de combinaison (ν1 + ν2 par exemple) : excitation simultanée de plusieurs vibrations fondamentales
II.3.2 - Types de mouvements de vibration et notations
En première approximation, les modes sont classés en fonction de deux paramètres :
Pour un groupement formé de plusieurs liaisons identiques :
II.3.3 les notations
Groupement fonctionnel formé d’une seule liaison (O-H, C=O..) :
δ : déformation dans les plan
γ : déformation hors du plan
Groupement formé de plusieurs liaisons identiques
II.4 - Les vibrations de groupe
Des groupes d’une molécule tels que (C=O, C-O, O-H, C-N, N-H, etc...) peuvent être excitées presque indépendamment du reste de la molécule.
Les bandes sont positionnées à des fréquences voisines sur les spectres IR et sont caractéristiques de ces fonctions.
Des tables permettent d'attribuer les absorptions aux différents groupes chimiques présents.
Région<1600 cm-1 : région des empreintes digitales.
III - APPLICATIONS DE LA SPECTROSCOPIE DE VIBRATION DANS L’INFRAROUGE
III.1 Composés organiques et inorganiques
Etat gazeux, liquide ou solide
Plusieurs grands champs d'application
III.2 - Analyse fonctionnelle
Détermination des groupements fonctionnels d’une molécule :
alcool, aldéhyde, cétone, acide...
Détermination des liaisons entre les carbones d'une chaîne :
chaîne saturée, insaturée, caractère aromatique d'une molécule...
Exemple : Liaisons C-H
Vibrations des liaisons C-H dépendent de l’hybridation de l'atome de carbone portant l'hydrogène.
Liaisons identiques dans un groupement
(ex. C-H d’un CH3 ou d’un CH2)
vibrent simultanément à la même fréquence.
Groupement CH2
Groupement CH3
